1. Ruch stały prostoliniowy.
2. Ruch zmienny.
3. Ruch po okręgu.
4. Zasady dynamiki Newtona.
5. Zasada względności
Galileusza.
6. Siła bezwładności.
7. Rzut poziomy.
8. Pęd, moment pędu, zasada zachowania pędu i zasada
zachowania momentu pędu.
9. Energia i zasada zachowania energii.
10. Praca i moc.
11. Siła tarcia.
12. Moment bezwładności i twierdzenie
Steinera.
13. Zderzenia centralne.
14. Gęstość i ciężar właściwy.
15. Pole grawitacyjne.
16. Prędkości kosmiczne.
17. Elektrostatyka.
18. Atom wodoru według Bohra.
19. Kondensator.
20. Polaryzacja elektryczna.
21. Prąd elektryczny stały.
22. Pole magnetyczne.
23. Prąd zmienny.
24. Drgania.
25. Fale.
26. Optyka geometryczna.
27. Dualizm
korpuskularnofalowy.
28. Fizyka atomowa.
|
28. Fizyka atomowa.
28.1 Liczby kwantowe.
- Pierwsza liczba kwantowa (główna) - n - określa ona numer
i rozmiar powłoki, n = 1,2,3,...
- Druga liczba kwantowa (orbitalna (poboczna)) - l (el)
-odpowiedzialna jest za moment pędu atomu w danym stanie energetycznym,
l = 0,1,2,...,n-1
- Trzecia liczba kwantowa (magnetyczna) - m - związana z momentem
magnetycznym. Przyjmuje ona wartości od -l do +l (od minus el do plus
el)
- Czwarta liczba kwantowa (spinowa) - s -

Na każdej powłoce może znaleźć się maxymalnie elektronów.
28.2 Zakaz Pauliego.
Na tej samej powłoce w danym stanie energetycznym nie mogą znaleźć się
dwa elektrony o jednakowych liczbach kwantowych. Muszą się
różnić przynajmniej spinem.
28.3 Reguła Kleczkowskiego.
Z dwóch elektronów mniejszą energię ma ten, dla
którego suma liczb orbitalnej i głównej jest
mniejsza.
28.4 Reguła Hunda.
Elektrony na danym podpoziomie rozmieszczają się w taki sposób,
aby sumaryczny spina był jak najmniejszy.
28.5 Widmo.
28.5.1 Widmo
Jest to zbiór wszystkich częstotliwości wyemitowanych przez atom
podczas przejścia atomu z poziomów energetycznych wyższych na
ściśle określone.
Widmo to linie papilarne atomów.
Ze względu na sposób otrzymywania widma dzielimy na :
- emisyjne - dostarczamy energii i pobudzamy atom do świecenia
- absorbcyjne - powstaje przy przejściu światła białego przez daną
substancję. Typowym widmem absorbcyjnym jest widmo słoneczne - czarne
kreski oznaczają, że dana długość fali została zaabsorbowana, czyli
występuje pierwiastek absorbujący ją (zob.pkt.28.5.4).
Widmo ciągłe - jedna barwa przechodzi w drugą bez wyraźnej granicy
(morphing)
Widmo liniowe - barwne prążki na ciemnym tle (dla atomów w
stanie gazowym).
Widmo pasmowe - dla cieczy i zw. chemicznych.
Widmo słoneczne służy do określania składu chemicznego i
poziomów energetycznych.
Do badania widma służy spektrometr.
28.5.2 Serie widmowe.
Serie widmowe :
- l=1 - seria Lymana (leży w nadfiolecie)
- l=2 - seria Balmera (jedyna seria widzialna)
Wszystkie pozostałe serie leżą w podczerwieni:
- l=3 - seria Paschena
- l=4 - seria Phunda
- l=5 - seria Humpreysa
Każda seria jest ograniczona z obu stron.
28.5.3 Widmo promieniowania
rentgenowskiego.
Katoda lampy rentgenowskiej jest zbudowana z wolframu.
Widmo :

Widmo jest ciągłe i liniowe (charakterystyczne). Widmo ciągłe nie
zależy od materiału, z jakiego zbudowana jest katoda, od tego zależy
widmo liniowe. Graniczna długość fali (lGR)
zależy od różnicy
potencjałów(zob.pkt.27.12.1).
28.5.4 Skład Słońca. Widmo słoneczne.
Budowa Słońca.
Jest to typowe widmo absorbcyjne (zob.pkt.28.5.1). Ciemne linie to
linie Fraunhofera. Są to zaabsorbowane częstotliwości, co oznacza, że
występuje pierwiastek, który je zaabsorbował. Stopień
zaczernienia linii określa w procentach ilość tego pierwiastka.
Skład Słońca : H (73,8%), He (23,6%), C, Mg, CH, OH, NH, CN, Ca, Na,
Al, Ne, Si, Fe, Ar, Na.
Dotychczas zidentyfikowano około 75% linii Fraunhofera.
Budowa Słońca :

Wiatr słoneczny, korona słoneczna i chronosfera tworzą atmosferę
Słońca. W warstwie konwektywnej energia transportowana jest przez
konwekcję. W warstwie promienistej energia transportowana jest za
pomocą promieni gamma.
Reakcja, która zachodzi w Słońcu, to synteza wodoru w hel
(zob.pkt.28.18).
28.6 Klasyfikacja widmowa gwiazd
- klasyfikacja Herztsprunga i Russela.
| klasa |
temperatura
powierzchni oK |
| O |
powyżej 100 000 |
| B |
50 000 - 100 000 |
| A |
... |
| F |
... |
| G |
... |
| K |
... |
| M |
3 000 |
W każdej klasie występują charakterystyczne linie.
28.7 Jasność absolutna.
Jest to jasność gwiazdy, która znajduje się w odległości 10
parseków od obserwatora.
1 parsek » 31 bilionów km » 3,26 lat świetlnych.
28.8 Klasyfikacja Morgana Keena.
Klasyfikacja gwiazd według jasności :
I. nadolbrzymy
II. jasne olbrzymy
III.olbrzymy
IV.podolbrzymy
V. gwiazdy ciągu głównego i karły
VI.podkarły
VII.białe karły
W tej klasywikacji zabrakło czarnych dziur i gwiazd neutronowych
(pulsarów).
28.9 Tablica Mendelejewa.
Jest to układ okresowy pierwiastków. Każdy pierwiastek jest
opisany w następujący sposób :  , gdzie : , gdzie :
A - określa ilość nukleonów w jądrze (suma protonów i
neutronów);
Z - liczba porządkowa, związana z ładunkiem (liczba elektronów,
tyle samo co elektronów jest też protonów).
28.10 Jądro atomu.
Składa się z protonów obdarzonych ładunkiem + i neutronów
nie obdarzonych ładunkiem. W lekkich jądrach liczba protonów i
elektronów jest jednakowa. W ciężkich przeważa ilość
neutronów. Odpowiedzialne są za to siły jądrowe: występują one
tylko pomiędzy najbliższymi nukleonami - przyciągają się. Natomiast
siły elektrostatyczne działają odpychająco pomiędzy wszystkimi
protonami. Gdyby ilość protonów i neutronów w ciężkim
jądrze była jednakowa, przeważyłyby siły odpychające, i jądro
rozpadłoby się.
Siły jądrowe mają mały zasięg, ale są najsilniejsze od wszystkich sił w
przyrodzie.
Rozmiary jądra atomowego :
  . .
Oznaczenia:
r - promień jądra atomowego;
A - określa ilość nukleonów w
jądrze (suma protonów i neutronów)(zob.pkt.28.9).
28.11 Energia wiązania jądra
atomowego.
Przy obliczeniu masy jądra atomowego według wzoru :
 , ,
dojdziemy do
wniosku, że jest ona mniejsza od masy odczytanej z tablicy Mendelejewa.
Niedobór masy związany jest z energią wiązania. Energię tę
wyliczymy ze wzoru:
 . .
W przeliczeniu : 1 jednostka atomowa jest
równa 931 megaelektronowoltom. Ta energia to energia wiązania -
energia, która wydzieli się podczas łączenia nukleonów w
jądra atomowe, lub którą należy dostarczyć aby podzielić jądro
na nukleony.
Energia właściwa - energia wiązania atomowego przypadająca na jeden
nukleon :

Najważniejsza krzywa świata :

Oznaczenia:
A - określa ilość nukleonów w jądrze (suma protonów i
neutronów) (zob.pkt.28.9);
DE - energia wiązania;
EW - energia
właściwa.
28.12 Promieniowanie naturalne.
Jest to proces samoistnej emisji promieniowania korpuskularnego lub
elektromagnetycznego (gamma).
Cechy promieniowania :
- pierwiastki promieniotwórcze
świecą
- działa bakteriobójczo
- jonizuje otoczenie
- powoduje mutacje komórek
- powoduje reakcję chemiczną
(zaciemniają kliszę)
28.13 Prawo zaniku
promieniotwórczości.
Prawo :

Oznaczenia:
l - długość fali;
N - liczba atomów, które NIE uległy
rozpadowi;
N0 - początkowa liczba cząstek;
e - liczba e;
t - czas.
28.14 Czas połowicznego zaniku
promieniotwórczego.
Jest to czas, po którym połowa atomów pierwiastka
promieniotwórczego ulega rozpadowi.
Czas połowicznego zaniku :

Oznaczenia:
l - długość fali;
t - czas połowicznego zaniku.
28.15 Reakcje jądrowe - samoistne
rozpady promieniotwórcze.
Własności promieniowania.
28.15.1 Reakcje jądrowe - samoistne
rozpady promieniotwórcze.
Rozpad zachodzi bez ingerencji z zewnątrz.
Rozpad a :
Podczas tego rozpadu emitowana jest cząstka a.
Strumień cząstek a
emitowany podczas rozpadu promieniotwórczego nazywa się
promieniowaniem a.
Reakcja : 
Przykład reakcji : 
Rozpad b- :
Podczas tego rozpadu emitowana jest cząstka b-.
Jest to elektron.
Strumień cząstek b- emitowany podczas
rozpadu promieniotwórczego
nazywa się promieniowaniem b-.
Reakcja : 
Przykład reakcji : 
Rozpad b+ :
Podczas tego rozpadu emitowana jest cząstka b+.
Jest to pozytron.
Strumień cząstek b+ emitowany podczas
rozpadu promieniotwórczego
nazywa się promieniowaniem b+.
Reakcja : 
Ten rozpad zachodzi bardzo rzadko, gdyż wcześniej musi być pochłonięty
elektron z powłoki.
Rozpad g:
Podczas tego rozpadu emitowana jest cząstka g.
Jest to pozytron.
Strumień cząstek g emitowany podczas
rozpadu promieniotwórczego
nazywa się promieniowaniem g.
Reakcja : 
Oznaczenia:
A - określa ilość nukleonów w jądrze (suma protonów i
neutronów) (zob.pkt.28.9);
Z - liczba porządkowa, związana z
ładunkiem (liczba elektronów, tyle samo co elektronów
jest też protonów) (zob.pkt.28.9);
X - pierwiastek przed
rozpadem;
Y - pierwiastek po rozpadzie;
X* - pierwiastek z jądrem
wzbudzonym;
ne - antyneutrino elektronowe.
28.15.2 Własności promieniowania.
Własności promieniowania a :
- jest to strumień cząstek +;
- poruszają się z różnymi
prędkościami dużo mniejszymi od prędkości światła;
- mają dużą bezwładność;
- oddziaływuje z polem elektrycznym i
magnetycznym tak jak ładunek +;
- posiada cechy promieniowania
(zob.pkt.28.12);
- ze wszystkich rodzajów
promieniowania jest najmniej przenikliwe i ma najkrótszy zasięg.
Własności promieniowania b- :
- cząstka b to elektron;
- jest to strumień cząstek -
- cząstki b poruszają się z prędkościami
bliskimi prędkościami światła;
- są bardziej przenikliwe niż cząstki a;
- oddziaływują z polem elektrycznym i
magnetycznym tak jak ładunek ujemny;
- mają mniejszą bezwładność od cząstek a;
- posiada cechy promieniowania
(zob.pkt.28.12).
Własności promieniowania g :
- jest to strumień kwantów
promieniowania elektromagnetycznego o bardzo małej długości fali (rzędu
10-14 m);
- najbardziej przenikliwe ze wszystkich
rodzajów promieniowania (aby zatrzymać trzeba 0,5 m ołowiu);
- nie niesie ze sobą ładunki i nie
oddziaływuje z polem elektrycznym ani magnetycznym;
- posiada cechy promieniowania
(zob.pkt.28.12).
Oznaczenie promieniowania:

28.16 Izotopy promieniotwórcze.
Izotop - odmiana pierwiastka wyjściowego różniąca się od niego
liczbą neutronów. Izotopy mają te same właściwości chemiczne
przy zmieniających się właściwościach fizycznych.
28.17 Reakcje jądrowe. Wymuszone
reakcje rozpadu.
Rozpad wymuszamy bombardując atom cząstką a, protonem, neutronem,
deutronem, trytonem lub jądrem litu. Typowa reakcja rozpadu :
 , gdzie : , gdzie :
X - bombardowany pierwiastek;
x - cząstka, którą bombardujemy;
Y
- otrzymany pierwiastek;
y - wyemitowana cząstka podczas procesu rozpadu.
Podczas reakcji jądrowej są spełnione zasady zachowania energii, pędu i
masy. Cząstką, dzięki której najłatwiej zachodzi reakcja
jądrowa, jest neutron.
28.18 Synteza - reakcja
termojądrowa.
Synteza zachodzi wśród pierwiastków, których
liczba masowa A < 60. Synteza zachodzi w wysokiej temperaturze.
Przykładem syntezy jest reakcja zachodząca w Słońcu :

 - najbardziej energetyczny cykl - najbardziej energetyczny cykl

 - anihilacja - anihilacja
Energia słoneczna powstaje kosztem 4 wodorów.
28.19 Reakcja rozszczepienia.
Rozszczepieniu zachodzą te pierwiastki, których liczba masowa A
jest większa od 60. Typową reakcją rozszczepienia jest rozszczepienie
235U :
 . .
Jak widać, po zbombardowaniu 235U neutronem
nastąpiła reakcja,
w której powstały 2 nowe neutrony. Mogą one samoistnie wejść w
reakcję z następnymi atomami 235U, powodując
reakcję łańcuchową.
Zachodzi ona niekontrolowanie w bombach atomowych.
28.20 Jonizacja gazu.
Aby przez gaz popłynął prąd elektryczny, gaz musi być zjonizowany.
Czynniki jonizujące gaz :
- wysoka temperatura;
- promieniowanie jonizujące (a, b, g, X);
- pośrednio - silne pole elektryczne;
Jonizacja pośrednia - w dostatecznie dużym polu elektrycznym elektrony
się rozpędzają i zderzając się z atomami powodują ich jonizację.
28.21 Detekcja promieniowania
jądrowego.
Detekcja może zachodzić za pomocą dwóch metod :
1. śladowa - obserwowanie śladu. Wykorzystywane w :
- komorze Wilsona;
- komorze dyfuzyjnej;
- komorze pęcherzykowej;
- emulsjach jądrowych;
2. jonizacyjna - zliczanie impulsów, pomiar napięcia
lub natężenia prądów przepływających przez detektor.
Wykorzystywane w :
- komorze jonizującej;
- liczniku Geigera - Mullera;
- liczniku scentylacyjny;
- licznikach półprzewodnikowych;
Komora Wilsona :
Jest to zbiornik wypełniony parą przechłodzoną. Aby dłużej utrzymać
cząsteczkę wewnątrz komory, jest ona ustawiona w polu magnetycznym. Gdy
we wnętrzu komory pojawi się cząstka, powoduje ona skraplanie się pary,
co można zarejestrować. Komora Wilsona nadaje się do obserwacji każdego
rodzaju cząstek. Za pomocą wyznaczonego toru możemy określić stosunek
masy do ładunku lub prędkości cząstki.
Komora pęcherzykowa.
Zbudowana jest podobnie do komory Wilsona, jednak parę przechłodzoną
zastąpiono cieczą przegrzaną, np. ciekłym azotem. Poruszająca się
cząstka powoduje parowanie cieczy. Na parze osadzają się pęcherzyki,
które pozostawiają ślad toru cząsteczki. . Za pomocą
wyznaczonego toru możemy określić stosunek masy do ładunku lub
prędkości cząstki.
Emulsje jądrowe.
zawiesina bardzo rozdrobnionych halogenków srebra (bromku,
jodku, chlorku) w żelatynie w stosunku 4:1. W kliszach fotograficznych
stosunek ten wynosi 1:1.
Licznik Geigera-Mullera.
Jest to licznik cząstek jonizujących. Składa się z metalowej rurki z
izolowanym od niej drutem wolframowym naciągniętym wzdłuż jej osi.
Wewnątrz rurki znajduje się rozrzedzony gaz, między rurką i drutem
przyłożone jest napięcie. Wpadająca do licznika Geigera–Mullera cząstka
jonizująca powoduje wyładowanie elektryczne w gazie, odpowiednio
rejestrowane (słyszalny stuk); impulsy elektryczne pochodzące od
wyładowań są następnie zliczane. Licznik Geigera-Mullera odznacza się
dużą czułością; jest stosowany m.in. w ochronie radiologicznej. Licznik
wykrywa promieniowanie a i b w 100%, natomiast promieniowanie g tylko w
0,1%, i dlatego się go nie stosuje do wykrywania promieniowania g.
28.22 Reaktor jądrowy.
Reaktor :

Jest to urządzenie do przeprowadzania w sposób kontrolowany
łańcuchowej reakcji rozszczepienia jąder atomowych (reakcja jądrowa).
Reakcja zachodzi w znajdującym się w rdzeniu reaktora paliwie jądrowym
(uran 235 lub 233, pluton 241 lub 239), a jej przebieg regulują pręty
kontrolne (wychwytując nadmiar neutronów, zapobiegają zbytniemu
rozwinięciu się reakcji łańcuchowej). Do spowalniania neutronów
– w celu ułatwienia reakcji z jądrami niektórych
pierwiastków – w rdzeniu znajduje się moderator (grafit, zwykła
woda, ciężka woda, beryl). Reaktory jądrowe służą jako źródło
energii (np. w elektrowniach jądrowych), źródło promieniowania
neutronowego do produkcji radioizotopów (izotopy) i wytwarzania
materiałów rozszczepialnych oraz są stosowane do celów
badawczych. W reaktorze na rysunku energia powstała w reakcji jest
transportowana przez ciecz chłodzącą do turbiny prądotwórczej.
Pierwszy reaktor jądrowy został uruchomiony 1942 w Chicago pod
kierunkiem E. Fermiego.
28.23 Cząstki elementarne.
(niedokończone)
28.24 Oddziaływania w przyrodzie.
W przyrodzie występują 4 podstawowe oddziaływania :
Grawitacyjne - podlegają mu wszystkie cząstki. Cząsteczki w trakcie
tego oddziaływania przekazują sobie grawiton :
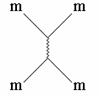
To oddziaływanie jest najsłabsze, ale ma największy zasięg.
Elektromagnetyczne - oddziaływanie cząstek naładowanych, których
moment magnetyczny jest różny do 0. Cząstką przekazywaną podczas
tego
oddziaływania jest foton. Siła tego oddziaływania jest nawet duża, lecz
ma mały zasięg.
Słabe - oddziaływanie pomiędzy wszystkimi cząstkami za wyjątkiem
fotonów. Zachodzi w odległości 10-15m. Cząstką przekazującą jest
bozon :

Silne - jądrowe - jest bardzo silne, ale najkrótsze (10-15m).
Zachodzi między kwarkami.
28.25 Wielka unifikacja oddziaływań
fizycznych.

28.26 Bomba atomowa i wodorowa.
Schemat :

Paliwem (ładunkiem atomowym) jest U233, U235 lub pluton. W bombie
atomowej następuje rozszczepienie. Mechanizm wywołujący wybuch
uruchamia zapalnik. Eksploduje zwykły materiał wybuchowy co powoduje
zetknięcie się dwóch części ładunku atomowego. Masa krytyczna
zostaje przekroczona i następuje niekontrolowana łańcuchowa reakcja
rozszczepiania jąder - czyli właściwy wybuch.
Przy wybuchu bomby wodorowej następuje synteza jąder izotopów
wodoru - do tego potrzebna jest wysoka temperatura. Taką temperaturę
można uzyskać przy wybuchu bomby atomowej. Tak więc „zapalnikiem” bomby
wodorowej jest bomba atomowa.
Skutki wybuchu bomby atomowej :
- promieniowanie cieplne;
- fala uderzeniowa;
- skażenie promieniotwórcze, co
powoduje choroby popromienne (białaczka, choroby soczewki oka) i
mutacje.
|
|
|






 , gdzie :
, gdzie :
 .
. ,
, .
. 










 , gdzie :
, gdzie :

 - najbardziej energetyczny cykl
- najbardziej energetyczny cykl
 - anihilacja
- anihilacja .
. 



